

溶解_科学小屋
溶解
2022-02-27 22:43:27 浏览:468 作者:管理员

溶解
广义上说,超过两种以上物质混合而成为一个状态的均匀相的过程称为溶解。而狭义的溶解指的是一种液体对于固体/液体/或气体产生物理或化学反应使其成为分子状态的均匀相的过程称为溶解。溶液并不一定为液体,可以是固体、液体、气体。比如均匀的合金和空气都可以称为溶液。当两种物质互溶时,一般把质量大的物质称为溶剂(如有水在其中,一般习惯将水称为溶剂)。
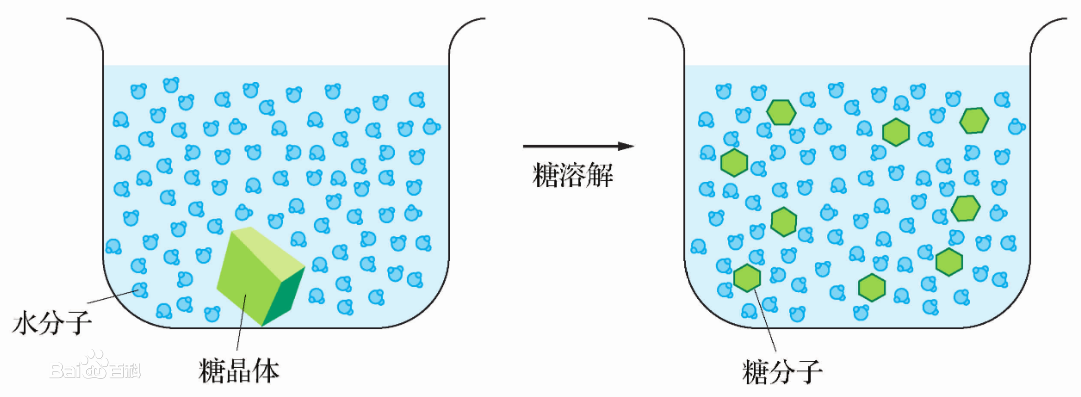
简述
物质溶解于水,通常经过两个过程:一种是溶质分子(或离子)的扩散过程,这种为物理过程需要吸收热量;另一种是溶质分子(或离子)和溶剂(水)分子作用,形成溶剂(水合)分子(或水合离子)的过程,这种过程是化学过程,放出热量。当放出的热量大于吸收的热量时,溶液温度就会升高,如浓硫酸、氢氧化钠等;当放出的热量小于吸收的热量时,溶液温度就会降低,如硝酸铵等;当放出的热量等于吸收的热量时,溶液温度不变,如氯化钠、蔗糖等。
固体溶质进入溶液后,首先发生微粒(分子或离子)的扩散(吸热)过程,接着是形成水合离子或水合分子的水合过程(放热)。这里有化学键的破坏和形成,严格说都是物理-化学过程。其实对于强电解质来说,溶解和电离是难以截然分开的,因为离子的扩散就是电离。不过对于弱电解质说来,首先是扩散成分子(吸热),然后在水分子作用下,化学键被破坏而电离成为自由离子(水合的)(这里总体表现是吸热还是放热要看破坏化学键需要的能量多,还是水合释放能量多了)。
假如是非电解质,那么溶解就是扩散与形成水合分子两个过程了。
一些溶质溶解后,会改变原有溶剂的性质,如氯化钠溶解在水中,电离为自由移动的钠离子与氯离子,故形成的溶液具有导电性(纯水不导电);乙二醇溶解在水中,可降低水的凝固点。
评论区
共 0 条评论
- 这篇文章还没有收到评论,赶紧来抢沙发吧~




